La Commissione Europea ha approvato dupilumab per il trattamento dell’orticaria cronica spontanea (CSU) da moderata a grave nei bambini dai due agli undici anni con risposta inadeguata agli antistaminici H1 (H1AH) e non precedentemente trattati con terapia anti-immunoglobulina E (IgE). La decisione della CE amplia la precedente indicazione, già approvata per adulti e adolescenti a partire dai 12 anni di età.
Dupilumab è un anticorpo monoclonale completamente umano sviluppato da Sanofi e Regeneron. Nei bambini dai due agli undici anni con orticaria cronica spontanea, sintomatici nonostante il trattamento con antistaminici H1, il farmaco viene somministrato per via sottocutanea in base all’età e al peso.
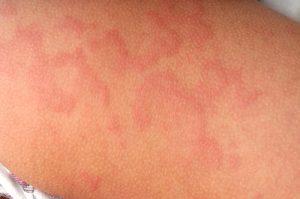
L’orticaria cronica spontanea è una malattia cutanea cronica e infiammatoria, causata in parte da un’infiammazione di tipo 2, che provoca la comparsa improvvisa di pomfi debilitanti e prurito ricorrente. Il trattamento di prima linea è rappresentato dagli antistaminici H1, che agiscono sui recettori H1 per controllare i sintomi. Tuttavia, in molti pazienti la malattia rimane non controllata nonostante la terapia e le opzioni alternative sono limitate.
“Le precedenti opzioni di trattamento per bambini più piccoli con orticaria cronica spontanea lasciavano molti pazienti con una malattia non controllata, caratterizzata dalla comparsa imprevedibile di prurito e pomfi che continuavano a condizionare fortemente la loro vita quotidiana”, spiega Alyssa Johnsen, Global Therapeutic Area Head, Immunology Development Sanofi, “Dupilumab, che inibisce la segnalazione di IL4 e IL13, due dei fattori chiave e fondamentali nel sostenere l’infiammazione di tipo 2, offre un approccio unico nel suo genere per affrontare l’orticaria cronica spontanea nei bambini piccoli. Questa approvazione dimostra il nostro impegno ad estendere il valore di dupilumab a tutti coloro che possono beneficiarne, inclusi i bambini piccoli”
Gli studi clinici
L’approvazione nell’UE si basa sui dati del programma di sviluppo clinico LIBERTY-CUPID. Il dossier include l’estrapolazione dei dati di efficacia negli adulti provenienti da due studi di fase III (Studio A e Studio C), integrati da dati farmacocinetici, di sicurezza ed efficacia derivati dallo studio di fase III CUPIDKids, a braccio singolo, condotto in pazienti pediatrici di età compresa tra 2 e 11 anni affetti da orticaria cronica spontanea.
Negli studi A e C, dupilumab ha dimostrato di ridurre in modo significativo l’attività della malattia – valutata attraverso un endpoint composito basato su prurito e pomfi – nonché le singole misure di gravità di questi sintomi rispetto al placebo alla settimana 24. Il trattamento ha inoltre aumentato la percentuale di pazienti con malattia ben controllata e con risposta completa rispetto al placebo nello stesso intervallo temporale.
Sicurezza della terapia
I risultati di sicurezza degli studi A, C e CUPIDKids sono risultati generalmente coerenti con il profilo di sicurezza noto di dupilumab nelle indicazioni dermatologiche approvate. Le reazioni avverse più comuni sono state reazioni al sito di iniezione, congiuntivite, congiuntivite allergica, artralgia, herpes orale ed eosinofilia. Per quanto riguarda le reazioni correlate al sito di iniezione, come indurimento, dermatite, lividi o ematomi, sono state osservate negli studi su adulti e adolescenti.
L’evento avverso più frequentemente osservato con dupilumab (=5%), rispetto al placebo nello Studio A e negli studi su adulti e adolescenti con orticaria cronica spontanea, è stato il COVID-19. I dati di sicurezza nei bambini dai due agli undici anni sono risultati generalmente coerenti con quelli osservati negli adulti e negli adolescenti.
“I bambini piccoli che soffrono di orticaria cronica spontanea spesso sperimentano un’improvvisa serie di episodi di prurito incessante e pomfi visibili durante gli anni critici della loro crescita e sviluppo”, conclude George D. Yancopoulos, Board co-Chair, President and Chief Scientific Officer Regeneron. “Essendo il primo e unico farmaco mirato per bambini piccoli nell’UE con CSU, dupilumab ha il potenziale per diventare il nuovo standard di cura per coloro che rimangono sintomatici nonostante altri trattamenti disponibili. Dupilumab è l’anticorpo monoclonale brand più utilizzato al mondo, e questa quarta approvazione per bambini piccoli con malattie croniche causate in parte dall’infiammazione di tipo 2 rende disponibile la sua efficacia comprovata e il suo profilo di sicurezza a lungo termine a un’altra popolazione vulnerabile che ne ha bisogno.”